新合生物迎来里程碑进展 mRNA肿瘤新抗原疫苗获IND受理
2023年3月4日,深圳市新合生物医疗科技有限公司提交的mRNA肿瘤新抗原疫苗XH101注射液的新药临床试验(IND)申请获得国家药品监督管理局药品审评中心(CDE)受理【受理号:CXSL2300170】,新合生物迎来RNA肿瘤治疗领域的里程碑进展。
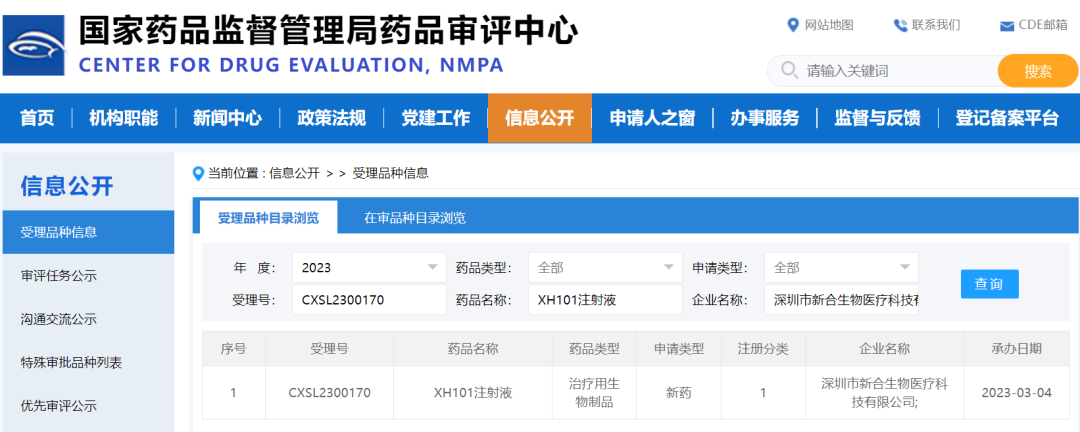
XH101注射液IND申请受理信息
XH101注射液是新合生物First in Class 靶向胃癌公共新抗原的治疗性mRNA肿瘤疫苗。该公共新抗原是新合生物通过自主研发的肿瘤新抗原预测算法平台、免疫原性Elispot验证平台及细胞杀伤平台,从大量胃癌患者中筛选、预测、验证出的一段免疫原性强、覆盖度广的肿瘤公共新抗原序列。临床前研究数据显示XH101注射液能够有效激发患者的T细胞免疫应答及肿瘤细胞杀伤效应,具有显著的临床治疗潜力。

新合生物疫苗生产车间
胃癌是一种起源于胃黏膜上皮的恶性肿瘤,是我国较为高发的的恶性肿瘤之一。据国际癌症研究机构(IARC)统计,2020年全球约有110万胃癌病例,中国患者占据其中的43.9%,约48万例,位居全球第一。数据显示,2020年中国胃癌新发病例数高达48万,死亡病例数超过37万,亟需创新疗法缓解这一公共难题。
在此背景下,新合生物依托前沿的AI+RNA技术和优秀的研发团队,针对胃癌自主研发了mRNA肿瘤公共新抗原疫苗XH101注射液。与传统药物相比,该疫苗具有更强的免疫原性,可诱发人体天然的免疫反应,不仅可以缩短疫苗制备周期,降低患者的治疗成本,还可以在患者体内产生持久有效的免疫记忆,为肿瘤防复发、防转移提供可能。同时,XH101注射液对晚期肿瘤和转移性肿瘤,还可起到有效抑制作用。

新合生物疫苗研发实验室
未来,新合生物希望通过持续研发为患者提供更多安全、有效的RNA创新药物,高质量地推动RNA创新药临床转化和应用,解决未被满足的临床需求,早日为患者带来更多、更优的治疗选择。

本文地址:http://www.cnzhilian.com/kuaixun/2023-03-07/631121.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 上一篇:融数赋智 健康随行 中兴通讯亮相中华医院信息网络大会
- 下一篇:返回列表
- 新合生物迎来里程碑进展 mRNA肿瘤新抗原疫苗获IND受理2023-03-07 14:37:54
- 融数赋智 健康随行 中兴通讯亮相中华医院信息网络大会2023-03-07 14:37:19
- 大流行后,如何重建我们的心理健康?2023-03-07 12:00:04
- 潜伏在我身体里40年的病毒,又“复活”了2023-03-07 12:00:04
- 甲流肆虐,该如何应对?现在打疫苗来得及吗?2023-03-07 12:00:01
-

 70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
2022-11-07
-

 梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
2022-09-08
-
烟台今天已封闭的小区 烟台现在封闭小区名单有哪些
2022-10-12 09:07:30
-
张家界桑植新娘吴梅婚纱照事件完整版 看女主出轨聊天内容视频
2022-11-11 14:27:00
-
目前南岸区及江北封闭小区名单有哪些 看最新封控通告
2022-11-11 14:49:26
-
无人售货机功能(无人自动售货机操作方法介绍)
2022-07-27 08:41:09
-
2022南宁封控小区名单表 南宁最新封闭小区名单2022年8月什么情况
2022-08-26 09:52:30


